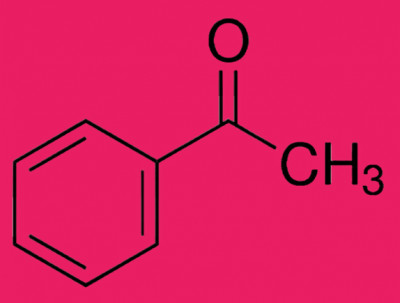
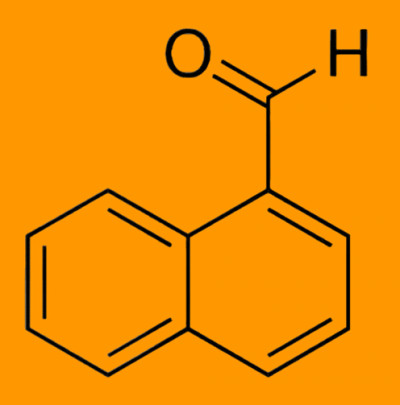
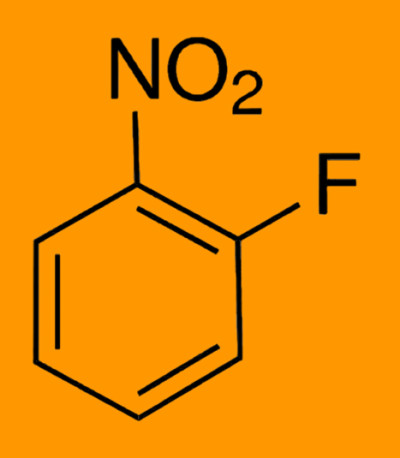
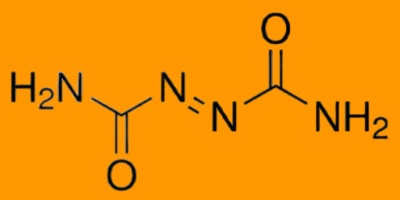
تلوریم یک عنصر شیمیایی با نماد Te و عدد اتمی 52 است. این یک متالوئید شکننده، کمی سمی، کمیاب و نقرهای سفید است. تلوریم از نظر شیمیایی با سلنیوم و گوگرد مرتبط است که هر سه آنها کالکوژن هستند . گاهی اوقات به شکل بومی به عنوان کریستال های عنصری یافت می شود. تلوریم در کل کیهان بسیار رایج تر از زمین است. نادر بودن شدید آن در پوسته زمین، قابل مقایسه با پلاتین ، تا حدی به دلیل تشکیل یک هیدرید فرار است.که باعث شد تلوریم به عنوان گاز در طول تشکیل سحابی داغ زمین در فضا گم ش
ترکیبات حاوی تلوریوم برای اولین بار در سال 1782 در یک معدن طلا در Kleinschlatten ، ترانسیلوانیا (زلاتنا، رومانی کنونی ) توسط کانی شناس اتریشی فرانتس-ژوزف مولر فون رایششتاین کشف شد، اگرچه این مارتین هاینریش کلاپروت بود که عنصر جدید را در سال 1798 به نام تیلوس نامگذاری کرد. 'زمین'. کانی های تلورید طلا قابل توجه ترین ترکیبات طبیعی طلا هستند. با این حال، آنها منبع تجاری مهمی از تلوریوم نیستند که معمولاً به عنوان محصول جانبی تولید مس و سرب استخراج می شود.
از نظر تجاری، استفاده اولیه از تلوریوم مس (مس تلوریوم ) و آلیاژهای فولادی است که ماشینکاری را بهبود میبخشد . کاربرد در پنل های خورشیدی CdTe و نیمه هادی های تلورید کادمیوم نیز بخش قابل توجهی از تولید تلوریم را مصرف می کند. تلوریم یک عنصر حیاتی فناوری در نظر گرفته می شود .
تلوریوم عملکرد بیولوژیکی ندارد، اگرچه قارچ ها می توانند آن را به جای گوگرد و سلنیوم در اسیدهای آمینه مانند تلوروسیستئین و تلورومتیونین استفاده کنند. در انسان، تلوریم تا حدی به دی متیل تلورید ، (CH 3 ) 2 Te متابولیزه می شود، گازی با بوی سیر مانند که در تنفس قربانیان قرار گرفتن در معرض تلوریوم یا مسمومیت بازدم می شود.
خصوصیات
خواص فیزیکی
تلوریم دارای دو آلوتروپ کریستالی و آمورف است. هنگامی که تلوریم کریستالی است، نقره ای مایل به سفید با درخشندگی فلزی است. بلورها مثلثی و کایرال هستند ( گروه فضایی 152 یا 154 بسته به کایرالیته)، مانند شکل خاکستری سلنیوم . این یک متالوئید شکننده است و به راحتی پودر می شود. تلوریم آمورف یک پودر قهوه ای سیاه است که با رسوب آن از محلول اسید تلوروس یا اسید تلوریک (Te(OH) 6 ) تهیه می شود. تلوریم نیمه هادی است که رسانایی الکتریکی بیشتری را در جهات خاص نشان می دهد.تراز اتمی ؛ رسانایی زمانی که در معرض نور قرار می گیرد کمی افزایش می یابد (رسانایی نوری ) . هنگامی که مذاب، تلوریم به مس، آهن و فولاد ضد زنگ خورنده است . از کلکوژن ها (عناصر خانواده اکسیژن)، تلوریم بالاترین نقطه ذوب و جوش را به ترتیب با 722.66 K (449.51 درجه سانتی گراد) و 1261 K (988 درجه سانتی گراد) دارد.
خواص شیمیایی
تلوریم کریستالی متشکل از زنجیره های مارپیچ موازی اتم های Te با سه اتم در هر نوبت است. این ماده خاکستری در برابر اکسیداسیون توسط هوا مقاومت می کند و فرار نیست.
ایزوتوپ ها
مقاله اصلی: ایزوتوپ های تلوریم
تلوریم طبیعی دارای هشت ایزوتوپ است. شش تا از این ایزوتوپ ها، ۱۲۰ Te، ۱۲۲ Te، ۱۲۳ Te، ۱۲۴ Te، ۱۲۵ Te و ۱۲۶ Te پایدار هستند. دو مورد دیگر، 128 Te و 130 Te، کمی رادیواکتیو هستند، با نیمه عمر بسیار طولانی، شامل 2.2 × 10 24 سال برای 128 Te. این طولانی ترین نیمه عمر شناخته شده در میان تمام پرتوزاها است و حدود 160 تریلیون ( 1012 ) برابر سن جهان شناخته شده است.. ایزوتوپ های پایدار تنها 33.2 درصد از تلوریم طبیعی را تشکیل می دهند.
31 رادیو ایزوتوپ مصنوعی دیگر از تلوریم با جرم اتمی بین 104 تا 142 و با نیمه عمر 19 روز یا کمتر شناخته شده است. همچنین 17 ایزومر هسته ای با نیمه عمر تا 154 روز شناخته شده است. به استثنای بریلیوم-8 و شاخه های آلفای با تاخیر در برخی از هسته های سبک تر ، تلوریم ( 104 Te تا 109 Te) سبک ترین عنصر با ایزوتوپ های شناخته شده برای واپاشی آلفا است.
جرم اتمی تلوریم (127.60 g·mol -1 ) بیشتر از ید است (126.90 g·mol -1 )، عنصر بعدی در جدول تناوبی.
وقوع
با فراوانی پوسته زمین که با پوسته پلاتین (حدود 1 میکروگرم بر کیلوگرم) قابل مقایسه است، تلوریم یکی از نادرترین عناصر جامد پایدار است. در مقایسه، حتی تولیوم ، نادرترین لانتانیدهای پایدار دارای فراوانی پوسته 500 میکروگرم بر کیلوگرم است (به فراوانی عناصر شیمیایی مراجعه کنید ).
این نادر بودن تلوریم در پوسته زمین بازتاب فراوانی کیهانی آن نیست. تلوریم در کیهان فراوانتر از روبیدیم است، اگرچه روبیدیم در پوسته زمین 10000 برابر بیشتر است. گمان میرود که نادر بودن تلوریم در زمین ناشی از شرایطی است که در طی مرتبسازی پیش از تجمع در سحابی خورشیدی رخ میدهد، زمانی که شکل پایدار عناصر خاص، در غیاب اکسیژن و آب ، توسط قدرت تقلیل هیدروژن آزاد کنترل میشد . تحت این سناریو، عناصر خاصی که هیدریدهای فرار را تشکیل می دهند ، مانند تلوریم، به شدت از طریق تبخیر این هیدریدها تخلیه می شوند. تلوریم و سلنیوم عناصر سنگینی هستند که در این فرآیند بیشتر تخلیه می شوند.
تلوریم گاهی به شکل اصلی خود (یعنی عنصری) یافت می شود، اما بیشتر به صورت تلوریدهای طلا مانند کالاوریت و کرنریت (دو چند شکل مختلف AuTe 2 ) ، پتزیت ، Ag 3 AuTe 2 ، و سیلوانیت ، AgAuTe 4 یافت می شود. . شهر تلوراید، کلرادو ، به امید اعتصاب تلورید طلا نامگذاری شد (که هرگز محقق نشد، اگرچه سنگ فلزی طلا یافت شد). خود طلا معمولاً بدون ترکیب یافت می شود، اما زمانی که به عنوان یک ترکیب شیمیایی یافت می شود، اغلب با تلوریم ترکیب می شود.
اگرچه تلوریم بیشتر با طلا یافت می شود تا به صورت غیر ترکیبی، اما حتی بیشتر به عنوان تلوریدهای فلزات رایج تر (مانند ملونیت ، NiTe2 ) ترکیب می شود. تلوریت طبیعی و کانی های تلورات نیز وجود دارند که از اکسیداسیون تلوریدها در نزدیکی سطح زمین تشکیل می شوند. برخلاف سلنیوم، تلوریم معمولاً جایگزین گوگرد در مواد معدنی نمیشود، زیرا در شعاع یونی تفاوت زیادی وجود دارد. بنابراین، بسیاری از کانیهای سولفیدی متداول حاوی مقادیر قابل توجهی سلنیوم و تنها آثاری از تلوریم هستند.
در هجوم طلا در سال 1893، معدنچیان در Kalgoorlie در جستجوی طلای خالص یک ماده پیریتی را دور انداختند و از آن برای پر کردن چالهها و ساختن پیادهرو استفاده میشد. در سال 1896، کشف شد که آن باطله کالاوریت است ، یک تلورید از طلا، و جرقه دوم طلایی را برانگیخت که شامل استخراج معادن در خیابان ها بود.
تاریخچه
حکاکی سیاه و سفید بیضی شکل مردی که به چپ نگاه می کند با روسری و کتی با دکمه های بزرگ.
کلاپروت عنصر جدید را نامگذاری کرد و کشف آن را به فون رایششتاین نسبت داد
تلوریوم ( لاتین تلوس به معنای زمین) در قرن هجدهم در یک سنگ معدن طلا از معادن Kleinschlatten (زلاتنای امروزی)، در نزدیکی شهر امروزی آلبا یولیا ، رومانی کشف شد. این سنگ به نام "Faczebajer weißes blättriges Golderz" (سنگ معدنی طلای برگدار سفید از Faczebaja، نام آلمانی Facebánya، اکنون Fața Băii در شهرستان آلبا ) یا antimonalischer Goldkies ( پیریت طلای آنتیمونیک) شناخته می شد . argent molybdique )، حاوی آنتیموان بومی است. [21] [22] در سال 1782 فرانتس ژوزف مولر فون رایششتاینکه در آن زمان به عنوان بازرس ارشد معادن اتریشی در ترانسیلوانیا خدمت می کرد، به این نتیجه رسید که سنگ معدن حاوی آنتیموان نیست بلکه سولفید بیسموت است . سال بعد، او گزارش داد که این اشتباه بود و سنگ معدن عمدتاً حاوی طلا و یک فلز ناشناخته است که بسیار شبیه آنتیموان است. مولر پس از یک بررسی کامل که سه سال به طول انجامید و شامل بیش از پنجاه آزمایش بود، وزن مخصوص این ماده معدنی را تعیین کرد و خاطرنشان کرد که وقتی فلز جدید گرم می شود، دود سفید با بویی شبیه تربچه از خود خارج می کند. که به اسید سولفوریک رنگ قرمز می بخشد; و اینکه وقتی این محلول با آب رقیق می شود رسوب سیاه رنگی دارد. با این وجود، او قادر به شناسایی این فلز نبود و نامهای aurum paradoxum (طلای متناقض) و metallum problematicum (فلز مشکلدار) را به آن داد، زیرا خواص پیشبینیشده برای آنتیموان را نشان نمیداد.
در سال 1789، یک دانشمند مجارستانی به نام Pál Kitaibel ، این عنصر را به طور مستقل در سنگ معدنی از Deutsch-Pilsen که به عنوان مولیبدنیت آرژانتیفر در نظر گرفته می شد، کشف کرد ، اما بعداً این عنصر را به مولر داد. در سال 1798 توسط مارتین هاینریش کلاپروت که قبلاً آن را از کانی کالاوریت جدا کرده بود نامگذاری شد .
در دهه 1960 کاربردهای ترموالکتریکی برای تلوریم (به عنوان بیسموت تلورید ) و آلیاژهای فولادی ماشینکاری آزاد افزایش یافت که استفاده غالب شد.
تولید
بیشتر Te (و Se) از رسوبات مس پورفیری به دست می آید ، جایی که در مقادیر کمی وجود دارد. این عنصر از لجن های آند از پالایش الکترولیتی مس تاول زده بازیابی می شود. این جزء غبارهای حاصل از تصفیه سرب کوره بلند است. تصفیه 1000 تن سنگ مس به طور معمول یک کیلوگرم (2.2 پوند) تلوریم به دست می دهد.
لجن های آند حاوی سلنیدها و تلوریدهای فلزات نجیب در ترکیباتی با فرمول M 2 Se یا M 2 Te (M = Cu, Ag, Au) هستند. در دمای 500 درجه سانتی گراد، لجن های آند با کربنات سدیم در زیر هوا برشته می شوند. یون های فلزی به فلزات احیا می شوند، در حالی که تلورید به تلوریت سدیم تبدیل می شود .
M 2 Te + O 2 + Na 2 CO 3 → Na 2 TeO 3 + 2 M + CO 2
تلوریت ها را می توان از مخلوط با آب شسته و معمولاً به صورت هیدروتلوریت HTeO 3 - در محلول وجود دارد. سلنیت ها نیز در طی این فرآیند تشکیل می شوند، اما می توان آنها را با افزودن اسید سولفوریک جدا کرد . هیدروتلوریت ها به دی اکسید تلوریم نامحلول تبدیل می شوند در حالی که سلنیت ها در محلول می مانند. [31]
HTEO-
3+ OH - + H 2 SO 4 → TeO 2 + SO2-
4+ 2 H 2 O
این فلز از اکسید (احیا شده) یا توسط الکترولیز یا با واکنش دی اکسید تلوریم با دی اکسید گوگرد در اسید سولفوریک تولید می شود.
TeO 2 + 2 SO 2 + 2H 2 O → Te + 2 SO2-
4+ 4 H +
تلوریم با درجه تجاری معمولاً به صورت پودر مش 200 به بازار عرضه می شود اما به صورت اسلب، شمش، چوب یا توده نیز موجود است. قیمت پایان سال تلوریم در سال 2000 14 دلار آمریکا به ازای هر پوند بود. در سالهای اخیر، قیمت تلوریم به دلیل افزایش تقاضا و عرضه محدود افزایش یافت و در سال 2006 به 100 دلار در هر پوند رسید . انرژی (DoE) کمبود عرضه تلوریوم را تا سال 2025 پیش بینی می کند.
تلوریم عمدتاً در ایالات متحده، پرو، ژاپن و کانادا تولید می شود. سازمان زمین شناسی بریتانیا اعداد تولید زیر را برای سال 2009 می دهد: ایالات متحده 50 تن ، پرو 7 تن، ژاپن 40 تن و کانادا 16 تن.
ترکیبات
همچنین به دسته بندی ترکیبات تلوریوم و کانی های تلورید مراجعه کنید
تلوریم متعلق به خانواده عناصر کالکوژن (گروه 16) در جدول تناوبی است که شامل اکسیژن ، گوگرد ، سلنیوم و پلونیوم نیز می شود : ترکیبات تلوریوم و سلنیوم مشابه هستند. تلوریم حالت های اکسیداسیون -2، +2، +4 و +6 را نشان می دهد که +4 رایج ترین آنهاست.
ترکیبات ارگانوتلوریوم
مقاله اصلی: شیمی ارگانوتلوریوم
تلوریوم به آسانی مشابه الکل ها و تیول ها با گروه عاملی -TeH که تلورول نامیده می شوند، تشکیل نمی دهد . گروه عملکردی –TeH نیز با استفاده از پیشوند tellanyl- نسبت داده می شود . مانند H2Te ، این گونه ها نسبت به از دست دادن هیدروژن ناپایدار هستند. Telluraetherها (R-Te-R) پایدارتر هستند، همانطور که تلوراکسیدها نیز پایدار هستند .
برنامه های کاربردی
بزرگترین مصرف کننده تلوریم متالورژی در آهن ، فولاد ضد زنگ ، مس و آلیاژهای سرب است. افزودن به فولاد و مس آلیاژی را تولید می کند که ماشینکاری بیشتری نسبت به موارد دیگر دارد. برای تقویت سرما برای طیفسنجی به چدن آلیاژ میشود ، جایی که وجود گرافیت آزاد رسانای الکتریکی با نتایج آزمایش انتشار جرقه تداخل دارد. در سرب، تلوریم استحکام و دوام را بهبود می بخشد و اثر خورندگی اسید سولفوریک را کاهش می دهد.
مقاله اصلی: شیمی ارگانوتلوریوم
ترکیبات ارگانوتلوریوم عمدتاً در زمینه تحقیق مورد توجه هستند. چندین مورد از جمله پیش سازها برای رشد اپیتاکسی فاز بخار متال آلی نیمه هادی های ترکیبی II-VI مورد بررسی قرار گرفته است . این ترکیبات پیش ساز شامل دی متیل تلورید ، دی اتیل تلورید، دی ایزوپروپیل تلوراید، دی آلیل تلورید و متیل آلیل تلورید می باشد. دی ایزوپروپیل تلورید (DIPTe) پیش ساز ارجح برای رشد CdHgTe در دمای پایین توسط MOVPE است. بیشترین خلوص متالارگانیک سلنیوم و تلوریم در این فرآیندها استفاده می شود. ترکیبات برای صنایع نیمه هادی و توسطتصفیه ترکیبی .
سابوکسید تلوریوم در لایه رسانه دیسکهای نوری قابل بازنویسی ، از جمله دیسکهای فشرده قابل بازنویسی ( CD-RW )، دیسکهای ویدئویی دیجیتالی قابل نوشتن مجدد ( DVD-RW ) و دیسکهای Blu-ray قابل نوشتن مجدد استفاده میشود .
دی اکسید تلوریوم برای ایجاد تعدیل کننده های آکوستو-اپتیک (AOTFs و AOBSs) برای میکروسکوپ کانفوکال استفاده می شود .
تلوریوم در تراشه های حافظه تغییر فاز توسعه یافته توسط اینتل استفاده می شود. تلورید بیسموت (Bi 2 Te 3 ) و تلورید سرب عناصر فعال دستگاه های ترموالکتریک هستند. تلورید سرب در آشکارسازهای مادون قرمز دور امیدوار کننده است.
فوتوکاتدها
تلوریم در تعدادی از فوتوکاتدهای مورد استفاده در لولههای فتومضریب کور خورشیدی و برای انژکتورهای نوری با روشنایی بالا که شتابدهندههای ذرات مدرن را هدایت میکنند، نشان داده میشود. فوتوکاتد Cs-Te، که عمدتاً Cs 2 Te است، آستانه انتشار نوری 3.5 eV دارد و ترکیبی غیر معمول از راندمان کوانتومی بالا (> 10٪) و دوام بالا در محیطهای خلاء ضعیف (طول ماهها تحت استفاده در الکترون RF را نشان میدهد. اسلحه). این امر باعث شده است که آن را به گزینه ای برای تفنگ های الکترونی تابش نور مورد استفاده در هدایت لیزرهای الکترون آزاد تبدیل کرده است. در این کاربرد، معمولاً در طول موج 267 نانومتر رانده می شود که سومین هارمونیک لیزرهای Ti-sapphire رایج است. فتوکاتدهای بیشتری حاوی Te با استفاده از سایر فلزات قلیایی مانند روبیدیم، پتاسیم و سدیم رشد کردهاند، اما آنها همان محبوبیتی را که Cs-Te داشته است، پیدا نکردهاند.
نقش بیولوژیکی
تلوریوم عملکرد بیولوژیکی شناخته شده ای ندارد، اگرچه قارچ ها می توانند آن را به جای گوگرد و سلنیوم در اسیدهای آمینه مانند تلوروسیستئین و تلورومتیونین بگنجانند . ارگانیسم ها تحمل بسیار متغیری نسبت به ترکیبات تلوریوم نشان داده اند. بسیاری از باکتریها، مانند سودوموناس آئروژینوزا ، تلوریت را جذب میکنند و آن را به تلوریم عنصری تبدیل میکنند که تجمع میکند و باعث تیره شدن مشخص و اغلب چشمگیر سلولها میشود. در مخمر، این کاهش توسط مسیر جذب سولفات انجام می شود. به نظر می رسد که تجمع تلوریوم بخش عمده ای از اثرات سمی را به خود اختصاص دهد. بسیاری از موجودات نیز تا حدی تلوریم را برای تشکیل دی متیل تلورید متابولیزه می کنند، اگرچه دی متیل دی تلوراید نیز توسط برخی گونه ها تشکیل می شود. دی متیل تلورید در چشمه های آب گرم در غلظت های بسیار کم مشاهده شده است.
تلوریت آگار برای شناسایی اعضای جنس corynebacterium ، به طور معمول Corynebacterium diphtheriae ، پاتوژن مسئول دیفتری استفاده می شود.
آزمیران به عنوان وارد کننده تلوریوم در ایران میتواند این محصول را در بسته بندی 25 گرمی و 100 گرمی 500 گرمی میتواند ارائه نماید لطفا با شماره تماس 09125344368 تماس حاصل فرمائید .