جوش شیرین یا بیکربنات سدیم با فرمول NaHCO۳ یکی از نمکهای سدیم در ترکیب با کربنیک اسید است که تنها یک هیدروژن اسیدی این ترکیب با سدیم جایگزین شدهاست. این ترکیب، بیبو و بیطعم است که کمی دارای خاصیت بازی است و به صورت پودر سپید یا بلورین است. بیکربنات جاذب رطوبت و بوگیر است.
این ترکیب که نام عامیانهاش «جوش شیرین» است، برای متخلخل کردن خمیر نان استفاده میشود و نیز برای کم کردن اسید معده و درمان سوز آن به کار میرود.
فرآوری
بیکربنات سدیم بیشتر به وسیلهٔ فرآیند سالوی ساخته میشود که همان واکنش کلرید سدیم، آمونیاک و کربن دیاکسید در آب است که بیکربنات سدیم به صورت رسوب به دست آمده پس از صاف کردن و خشک کردن با حرارت به کربنات سدیم تبدیل خواهد شد. سالانه نزدیک به ۱۰۰۰۰۰ تن جوش شیرین فرآوری میشود. (سال ۲۰۰۱)[۶] همچنین میتوان با عبور دادن گاز از درون محلول جوشان کربنات سدیم خالص یا محلول هیدروکسید سدیم، بیکربنات سدیم را به شکل رسوب تهنشین شده به دست آورد.
ویژگیها
جوش شیرین در آب یک آمفوتر است. یعنی در آب میتواند به عنوان اسید یا باز رفتار کند. رفتار اسیدی آن به سبب وجود هیدروژن در ترکیبش است که در صنایع مختلف به عنوان آزادکننده کاربرد دارد.
حلالیت
در دمای معمولی ۱۰٫۳ گرم از این ماده در ۱۰۰ گرم آب حل میشود. اما در اتانول به مقدار کم محلول است.
کاربرد
بیشترین استفاده از بیکربنات سدیم در فرآوری انواع بکینگ پودر است. مقدار اضافی از خمیر جوش شیرین بطور مؤثر در پاک کردن و سائیدن سطوح میتواند استفاده گردد. استفاده از این ماده در ترکیب خمیر دندان به رفع تدریجی لکههای دندان و سفید شدن آنها کمک میکند. در صنایع غذایی، تولید نوشابههای گازدار به عنوان منبع، صنایع پاک کنندههای خانگی و در کپسولهای خاموش کننده آتش بکار میرود. همچنین به عنوان باز دارنده در مواد منفجره استفاده میشود. در صنعت نساجی برای عمل آوردن نخهای پشمی و ابریشمی استفاده میشود. همچنین میتواند به عنوان پاک کننده و ساینده ملایم در صورتی که ایجاد حساسیت نکند برای زیبایی پوست بکار رود.ضمن آنکه جوش شیرین به عنوان یک مکمل خوراکی در جیره غذایی دام و طیور می تواند در جهت جلوگیری از اختلالات متابولیکی و تغذیه ای بکار برده شود.
ایمنی
خوردن این ماده بیضرر است مگر اینکه به مقدار خیلی زیاد باشد. بوییدن آن ممکن است سبب سوزش بینی یا گلو شود. در اثر تماس با پوستهای حساس ممکن است باعث خارش یا سوزش پوست شود. در اثر تماس با چشم ممکن است سبب ایجاد سوزش و سرخی در چشم شود.
استفاده از جوش شیرین در پخت همه نوع نان و شیرینی مضر است.
| جوش شیرین | |
|---|---|
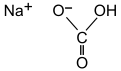 |
|
 |
 |
 |
|
| نامهای دیگر | Baking soda, bicarbonate of soda, nahcolite, sodium bicarbonate, sodium hydrogencarbonate |
| شناساگرها | |
| CAS | 144-55-8 |
| پابکم | 516892 |
| کماسپایدر | 8609 |
| UNII | 8MDF5V39QO |
| شماره EINECS | |
| دراگبانک | DB01390 |
| KEGG | C12603 |
| MeSH | Sodium+bicarbonate |
| ChEBI | CHEBI:32139 |
| ChEMBL | CHEMBL1353 |
| شماره RTECS |
VZ0950000
|
| کد اِیتیسی | B05,B05XA02, الگو:ATCvet |
| بیلشتین | 4153970 |
| Jmol-3D images | Image 1 |
| خصوصیات | |
| فرمول شیمیایی |
NaHCO3
|
| جرم مولی |
84.007 g mol−1
|
| Exact mass | 83.982338573 g mol−1 |
| شکل ظاهری | White crystals |
| بوی | odorless |
| چگالی | 2.20 g cm−3[۱] |
| دمای ذوب |
50 °C, 323 K, 122 °F (decomposes)
|
| دمای جوش |
851 °C, 1124 K, 1564 °F
|
| محلول در آب | 9 g/100 mL
69 g/L (0 °C)[۲] |
| محلول | insoluble in اتانول |
| log P | -0.82 |
| اسیدی (pKa) | 10.329[۴]
6.351 (carbonic acid)[۴] |
| ضریب شکست (nD) | 1.3344 |
| داروشناسی | |
| Routes of administration |
Intravenous, oral |
| ترموشیمی | |
| آنتالپی استاندارد تشکیل ΔfH |
−948 kJ·mol−1[۵] |
| آنتروپی مولار استاندارد S |
102 J·mol−1·K−1[۵] |
| ترکیبات مرتبط | |
| آنیونهای دیگر | سدیم کربنات |
| کاتیونهای دیگر | بیکربنات آمونیوم بیکربنات پتاسیم |
| ترکیبات مرتبط | سدیم بیسولفات سدیم فسفات |
| تمامی دادهها مربوط به شرایط استاندارد(در °C۲۵ و kPa۱۰۰) است، مگر آنکه خلاف آن ذکر شده باشد. | |
منبع ویکیپدیا
: